河南华智生物科技有限公司报告,由于企业生产的电动颈椎牵引装置的使用说明书及开关动作方向不合格,(涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》),企业对其生产的电动颈椎牵引装置主动召回。召回级别为三级。
召回原因简述:在医疗器械抽检中出现产品不合格(产品型号: JLB-800C, 编号:HZJLB800C1906001),涉及型号的产品说明书未指明有关废弃物、残渣等以及设备和附件在其使用寿命末期时的处理的任何风险。开关动作方向不符合GB/T4205的要求。
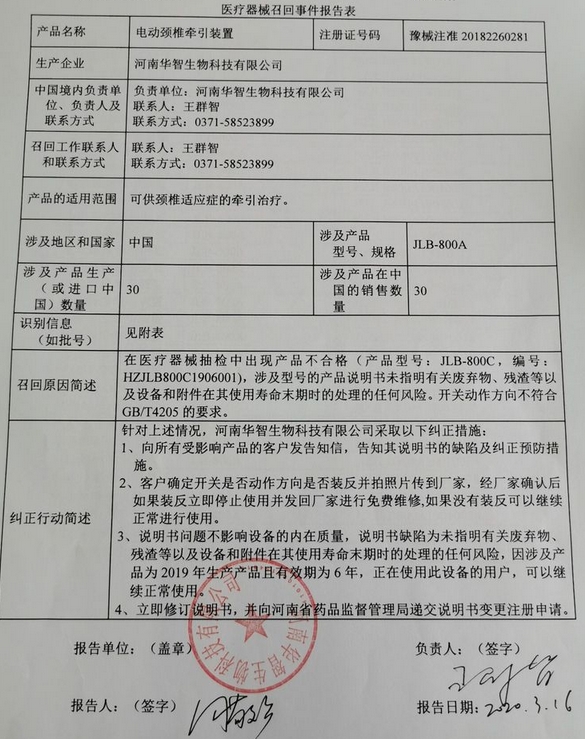
河南华智生物科技有限公司报告,由于企业生产的电动颈椎牵引装置的使用说明书及开关动作方向不合格,(涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》),企业对其生产的电动颈椎牵引装置主动召回。召回级别为三级。
召回原因简述:在医疗器械抽检中出现产品不合格(产品型号: JLB-800C, 编号:HZJLB800C1906001),涉及型号的产品说明书未指明有关废弃物、残渣等以及设备和附件在其使用寿命末期时的处理的任何风险。开关动作方向不符合GB/T4205的要求。
